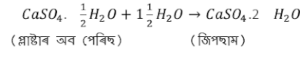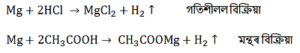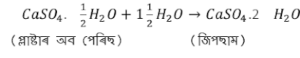NCERT class 10 science chapter 2: Acid Bases and Salts এছিড, ক্ষাৰক আৰু লৱন – অসমীয়াত সম্পূৰ্ণ সমাধান। আমি এই ব্লগত অসমৰ অসমীয়া মাধ্যমৰ ছাত্ৰ-ছাত্ৰীৰ বাবে ৭, ৮, ৯, ১০, ১১ আৰু ১২ শ্ৰেণীৰ বাবে বিনামূলীয়া NCERT সমাধান প্ৰদান কৰোঁ।
এই পৃষ্ঠাত আপুনি দশম শ্ৰেণীৰ বিজ্ঞান অধ্যায় ২: এছিড, ক্ষাৰক আৰু লৱনৰ সম্পূৰ্ণ প্ৰশ্ন আৰু উত্তৰৰ লগতে কিছুমান গুৰুত্বপূৰ্ণ অতিৰিক্ত পৰীক্ষামুখী চুটি প্ৰশ্ন আৰু উত্তৰ আমাৰ দ্বাৰা অন্তৰ্ভুক্ত কৰা হৈছে যিয়ে আপোনাক অধ্যায়টো অতি ভালদৰে বুজিবলৈ সহায় কৰিব।
Class 10 Science Chapter 2 Solutions – এছিড, ক্ষাৰক আৰু লৱন
(এছিড, ক্ষাৰক আৰু লৱন)
(In-Text Question Answers)
Question 1: তোমাক তিনিটা পৰীক্ষানল দিয়া হৈছে । সিহঁতৰ এটাত পাতিত পানী আৰু আন দুটাত ক্ৰমে এটা এছিড দ্ৰৱ আৰু এটা ক্ষাৰকীয় দ্ৰৱ আছে । যদি তোমাক কেৱল ৰঙা লিটমাছ কাগজ দিয়া হয়, তেন্তে প্ৰতিটো পৰীক্ষানলত থকা দ্ৰৱসমূহ কিদৰে চিনাক্ত কৰিবা ?
Answer: ধৰাহল পৰীক্ষানল তিনিটা A, B আৰু C ।
প্ৰথমে A পৰীক্ষানলটোত ৰঙা লিটমাছ কাগজটো দ্ৰৱীভূত কৰা হ’ল লিটমাছ কাগজৰ ৰঙৰ পৰিৱৰ্তন নহ’ল । গতিকে, পৰীক্ষানলটোত পাতিত পানী আছে ।
দ্বিতীয় পৰীক্ষানল B ত ৰঙা লিটমাছ কাগজটো দ্ৰৱীভূত কৰা হ’ল লিটমাছ কাগজটোৰ বৰণ নীলা হ’ল । গতিকে পৰীক্ষানলটোত ক্ষাৰকীয় দ্ৰৱ আছে । যিহেতু ক্ষাৰকে ৰঙা লিটমাছ নীলা কৰে ।
এই নীলা লিটমাছ কাগজটো তৃতীয় পৰীক্ষানল C ত ৱীভূত কৰাত ইয়াৰ বৰণ ৰঙালৈ পৰিৱৰ্তন হ’ল । গতিকে এই পৰীক্ষানলটোত এছিড দ্ৰৱ আছে ।
Question 2: দৈ আৰু টেঙা খাদ্যবস্তু পিতলৰ আৰু তামৰ পাত্ৰত থোৱা নহয় কিয় ?
Answer: ধাতুয়ে এছিডৰ লগত বিক্ৰিয়া কৰিলে ধাতবীয় লৱণ আৰু হাইড্ৰ’জেন গেছ উৎপন্ন হয় । দৈ আৰু টেঙা খাদ্যবস্তু পিতলৰ আৰু তামৰ পাত্ৰত ৰাখিলে বিষাক্ত ধাতবীয় লৱণ আৰু হাইড্ৰ’জেন গেছ উৎপন্ন হয় । এই লৱণ আমাৰ শৰীৰৰ বাবে অনিষ্টকাৰী । সেই কাৰণে দৈ আৰু টেঙা খাদ্যবস্তু পিতলৰ আৰু তামৰ পাত্ৰত থোৱা নহয় ।
Question 3: এছিডে ধাতুৰ সৈতে বিক্ৰিয়া কৰিলে সাধাৰণতে কোনটো গেছ নিৰ্গত হয় ? এটা উদাহৰণেৰে সৈতে বুজাই লিখা । এই গেছটোৰ উপস্থিতি কিদৰে পৰীক্ষা কৰিবা ?
Answer: এছিডে ধাতুৰ সৈতে বিক্ৰিয়া কৰিলে সাধাৰণতে হাইড্ৰ’জেন গেছ নিৰ্গত হয় । এছিডে ধাতুৰ সৈতে বিক্ৰিয়াটো –
এছিড + ধাতু → ধাতবীয় লৱণ + হাইড্ৰ’জেন গেছ
উদাহৰণস্বৰূপে, মেগনেছিয়াম ধাতুৱে ছালফিউৰিক এছিডৰ সৈতে বিক্ৰিয়া কৰিলে মেগনেছিয়াম ছালফেট আৰু হাইড্ৰ’জেন গেছ উৎপন্ন হয় ।
Mg + H2SO4 → MgSO4 + H2 (তাপ)
উৎপন্ন হোৱা গেছটোক চাবোন পানীৰ মাজেৰে যাবলৈ দিলে আৰু এডাল জ্বলি থকা মম গেছ ভৰ্ত্তি বুদবুদ এটাৰ ওপৰত ধৰিলে বুদবুদবোৰ ফাটি যাব আৰু গেছটো নিজে জ্বলি যাব । এই গেছে হাইড্ৰ’জেনৰ উপস্থিতি বুজায় ।
Question 4: এটা ধাতৱ যৌগ A লঘু হাইড্ৰ’ক্লৰিক এছিডৰে সৈতে বিক্ৰিয়া কৰি বুৰবুৰনি সৃষ্টি কৰে । উৎপন্ন হোৱা গেছটোৱে এডাল জ্বলি থকা ম’ম নুমুৱায় । বিক্ৰিয়াটোত উৎপন্ন হোৱা এটা যৌগ কেলছিয়াম ক্ল’ৰাইড হ’লে বিক্ৰিয়াটোৰ বাবে সন্তুলিত সমীকৰণটো লিখা ।
Answer: ধাতৱ যৌগ ৰ সৈতে লঘু হাইড্ৰ’ক্লৰিক এছিডৰ সৈতে বিক্ৰিয়া কৰিলে কেলছিয়াম ক্ল’ৰাইড, কাৰ্বন-ডাই-অক্সাইড আৰু পানী উৎপন্ন হয় । আমি জানো, কাৰ্বন-ডাই-অক্সাইডে জুই নুমায় । গতিকে ইয়াৰ আসন্ন সমীকৰণটো হ’ব –
(MCO3)A
+ HCl → CaCl2 + CO2↑ + H2O
মুখ্য সমীকৰণটো হ’ব –
CaCO3
+ 2HCl → CaCl2 + CO2↑ + H2O
∴ A
যৌগটো কেলছিয়াম কাৰ্বনেট (CaCO3)।
Question 5: জলীয় দ্ৰৱত HCl, HNO3 ইত্যাদিয়ে কিয় আম্লিক ধৰ্ম দেখুৱায় কিন্তু এলকহল আৰু গ্লূক’জৰ দৰে যৌগৰ দ্ৰৱই আম্লিক ধৰ্ম নেদেখুৱায় ?
Answer: HNO3 আৰু HCl এছিডে পানীৰ লগত বিক্ৰিয়া কৰিলে হাইড্ৰনিয়াম আয়ন (H3O+) উৎপন্ন কৰে । সেইবাবে HNO3 আৰু HCl য়ে জলীয় দ্ৰৱত আম্লিক ধৰ্ম দেখুৱায় । ইয়াৰ সমীকৰণটো হল –
HCl + H2O
→ H3O+
+Cl−
HNO3
+ H2O → H3O+ + NO3−
আনহাতে, এলকহল আৰু গ্লূক’জৰ দৰে যৌগই পানীৰ লগত বিক্ৰিয়া কৰিলে হাইড্ৰক্সাইড আয়ন (OH−) উৎপন্ন কৰে । এইবোৰে হাইড্ৰনিয়াম আয়ন (H3O+) উৎপন্ন নকৰে । সেয়েহে এলকহল আৰু গ্লূক’জৰ দৰে যৌগৰ দ্ৰৱই আম্লিক ধৰ্ম নেদেখুৱায় ।
Question 6: এছিড এটাৰ জলীয়া দ্ৰৱই কিয় বিদ্যুৎ পৰিবহন কৰে ?
Answer: এছিডে পানীৰ লগত বিক্ৰিয়া কৰিলে কেটায়ন আৰু এনায়ন উৎপন্ন কৰে । দ্ৰৱত থকা এই আয়নবোৰৰ জৰিয়তে বিদ্যুত প্ৰবাহিত হয় । সেয়ে এছিড এটাৰ জলীয়া দ্ৰৱই বিদ্যুৎ পৰিবহন কৰে ।
Question 7: শুকান HCl গেছে কিয় শুকান লিটমাছ কাগজৰ ৰঙৰ পৰিৰ্ৱতন নঘটায় ?
Answer: এছিডে কেৱল জলীয়া দ্ৰৱতহে আয়ন উৎপন্ন কৰে । আয়ন থাকিলেহে লিটমাছ কাগজে ৰঙৰ পৰিৰ্ৱতন কৰে । সেইবাবে শুকান HCl গেছে শুকান লিটমাছ কাগজৰ ৰঙৰ পৰিৰ্ৱতন নঘটায়।
Question 8: এছিড এটা লঘু কৰোঁতে এছিড পানীত যোগ কৰিবলৈ কোৱা হয় কিন্তু পানী এছিডত যোগ কৰিবলৈ কোৱা নহয় কিয় ?
Answer: এছিড সদায় পানীতহে লাহে লাহে যোগ কৰিব লাগে আৰু এইটো কৰোঁতে দ্ৰৱটো একেলেথাৰিয়ে লৰাই থাকিব লাগে । কিন্তু যেতিয়া পানী এছিডত যোগ কৰা হয় তেতিয়া উৎপন্ন হোৱা তাপৰ বাবে মিশ্ৰটো বাহিৰলৈ ছিটিকি পৰিব পাৰে ফলত জুই লাগিব পাৰে । সেইবাবে পানী এছিডত যোগ কৰা নহয় ।
Question 9: এছিডৰ দ্ৰৱ এটা লঘু কৰোঁতে হাইড্ৰনিয়াম আয়ন (H3O+) ৰ গাঢ়তা কিদৰে পৰিৱৰ্তন হয় ?
Answer: এছিডে পানীৰ সৈতে বিক্ৰিয়া কৰিলে হাইড্ৰনিয়াম আয়ন (H3O+) উৎপন্ন হয় । যেতিয়া মিশ্ৰটো লঘু কৰা হয় ইয়াৰ আয়তন বাঢ়ি যায় কিন্তু আয়নৰ সংখ্যা একেই থাকে । গতিকে এছিডৰ দ্ৰৱ এটা যিমানেই লঘু কৰা হয় ইয়াত থকা হাইড্ৰনিয়াম আয়ন (H3O+) ৰ গাঢ়তাও কমি যায়।
Question 10: ছডিয়াম হাইড্ৰ’অক্সাইডৰ দ্ৰৱ এটাত অধিক ক্ষাৰক দ্ৰৱীভূত কৰিলে হাইড্ৰ’অক্সাইড আয়ন (OH−) ৰ গাঢ়তা কিদৰে পৰিৱৰ্তিত হ’ব ?
Answer: ছডিয়াম হাইড্ৰ’অক্সাইডে পানীৰ সৈতে বিক্ৰিয়া কৰিলে হাইড্ৰ’অক্সাইড আয়ন (OH−) উৎপন্ন হয় । ছডিয়াম হাইড্ৰ’অক্সাইডৰ দ্ৰৱ এটাত অধিক ক্ষাৰক দ্ৰৱীভূত কৰিলে প্ৰতি একক আয়তনত হাইড্ৰ’অক্সাইড আয়ন (OH−) ৰ গাঢ়তা কমি যায় ।
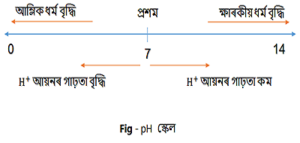
Question 11: তোমাৰ হাতত A আৰু B টা দ্ৰৱ আছে । দ্ৰৱ A ৰ pH ৰ মান 6 আৰু দ্ৰৱ B ৰ pH ৰ মান 8। কোনটো দ্ৰৱত হাইড্ৰ’জেন আয়নৰ গাঢ়তা বেছি ? কোনটো আম্লিক আৰু কোনটো ক্ষাৰকীয় ?
Answer: দ্ৰৱ এটাৰ pH ৰ মান যিমানে কম হয়, ইয়াত থকা হাইড্ৰ’জেন আয়নৰ গাঢ়তা সিমানে বেছি হয় । অথাৎ দ্ৰৱটোৰ আম্লিকতা বৃদ্ধি পায় আৰু ইয়াৰ লগতে ক্ষাৰকীয় গুণ হ্ৰাস পায় । গতিকে A দ্ৰৱত হাইড্ৰ’জেন আয়নৰ গাঢ়তা বেছি হ’ব আৰু ই আম্লিক । আনহাতে B দ্ৰৱটো ক্ষাৰকীয় হ’ব।
Question 12: দ্ৰৱ এটাৰ প্ৰকৃতিৰ ওপৰত H+ (aq) আয়নৰ গাঢ়তাৰ কি প্ৰভাৱ থাকে ?
Answer: এছিডৰ তীব্ৰতা উৎপাদিত H+ আয়নৰ গাঢ়তাৰ ওপৰত নিৰ্ভৰ কৰে । বেছিকৈ H+ আয়ন উৎপন্ন কৰা এছিডবোৰক তীব্ৰ এছি়ড আৰু কমকৈ H+ আয়ন উৎপন্ন কৰা এছিডবোৰক মৃদু এছি়ড বোলা হয় ।
Question 13: ক্ষাৰকীয় দ্ৰৱত H+ (aq) আয়ন থাকেনে ? যদি থাকে, তেন্তে ইহঁত কিয় ক্ষাৰকীয় ?
Answer: হয়, ক্ষাৰকীয় দ্ৰৱ বোৰতো H+(aq) আয়ন থাকে । কিন্তু ইয়াৰ গাঢ়তা OH− আয়নৰ গাঢ়তাতকৈ কম । ক্ষাৰকীয় দ্ৰৱত OH− আয়নৰ গাঢ়তা বেছি হোৱাৰ বাবে ইহঁত ক্ষাৰকীয় ধৰ্ম দেখুৱায়।
Question 14: মাটিত কি অৱস্থাত কৃষক এজনে পোৰা চূণ (কেলছিয়াম অক্সাইড) বা শিথিলিত চূণ (কেলছিয়াম হাইড্ৰক্সাইড) বা চক (কেলছিয়াম কাৰ্বনেট) প্ৰয়োগ কৰিব বুলি তোমালোকে ভাবা ?
Answer: যেতিয়া মাটিৰ গুণাগুণ কমি যায় অথাৎ pH ৰ মান কমি 7তকৈ কম হয়, তেতিয়া মাটিত গছ-গছনিৰ বৃদ্ধ ক্ৰমে কমি যায় । তেনে অৱস্থাত কৃষক এজনে মাটিৰ pHৰ মান প্ৰশম (pHৰ মান 7) কৰিবলৈ পোৰা চূণ (কেলছিয়াম অক্সাইড) বা শিথিলিত চূণ (কেলছিয়াম হাইড্ৰ’ক্সাইড) বা চক (কেলছিয়াম কাৰ্বনেট) আদি প্ৰয়োগ কৰে । ইয়াৰ ফলত গছ-গছনিৰ বৃদ্ধি হয়।
Question 15: যৌগ CaOCl2 ৰ সাধাৰণ নামটো কি ?
Answer: যৌগ CaOCl2 ৰ সাধাৰণ নাম ব্লিচিং পাউদাৰ ।
Question 16: ক্ল’ৰিনৰ সৈতে বিক্ৰিয়া কৰালে ব্লিচিং পাউদাৰ উৎপন্ন কৰা যৌগটোৰ নাম লিখা ।
Answer: শুকান শিথিলিত চূণ [Ca(OH)2]
ইয়াৰ বিক্ৰিয়াটো হ’ল –
Ca(OH)2 + Cl2 → CaOCl2
+ H2O
Question 17: কঠিন পানী কমল কৰাৰ কাৰণে ব্যৱহাৰ কৰা ছ’ডিয়াম যৌগটোৰ নাম লিখা ।
Answer: ছ’ডিয়াম কাৰ্বনেট (কাপোৰ ধোৱা ছডা ) ।
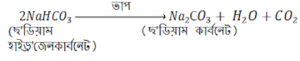
Question 18: ছ’ডিয়াম হাইড্ৰ’জেনকাৰ্বনেটৰ দ্ৰৱ এটা উত্তপ্ত কৰিলে কি হয়? বিক্ৰিয়াটোৰ সমীকৰণটো দিয়া ।
Answer: ছ’ডিয়াম হাইড্ৰ’জেনকাৰ্বনেটৰ দ্ৰৱ এটা উত্তপ্ত কৰিলে ছ’ডিয়াম কাৰ্বনেট, কাৰ্বন-ডাই-অক্সাইড আৰু পানী উৎপন্ন হয় । এই বিক্ৰিয়াটোৰ সমীকৰণটো হ’ল-
Question 19: প্লাষ্টাৰ অব পেৰিছ আৰু পানীৰ মাজৰ বিক্ৰিয়াটো দেখুৱাবলৈ এটা সমীকৰণ লিখা ।
Answer: প্লাষ্টাৰ অব পেৰিছ আৰু পানীৰ মাজৰ বিক্ৰিয়া হ’লে জিপছাম পোৱা যায় । ইয়াৰ সমীকৰণটো হ’ল –
————–
(ৰাসায়নিক বিক্ৰিয়া আৰু সমীকৰণ)
(Exercise Question Answers)
Question 1: এটা দ্ৰৱই ৰঙা লিটমাছ নীলা কৰিছে । ইয়াত pH হ’ব পাৰে –
(a) 1 (b) 4 (c) 5 (d) 10
Answer: (d) 10
Question 2: এটা দ্ৰৱই গুড়ি কৰি লোৱা কণীৰ খোলাৰ সৈতে বিক্ৰিয়া কৰি এটা গেছ উপন্ন কৰে । গেছটোৱে চূণপানী ঘোলা কৰে । দ্ৰৱটোত থাকে –
(a) NaCl (b) HCl (c) LiCl (d) KCl
Answer: (b) HCl
Question 3: NaOH দ্ৰৱ এটাৰ 10 mL এ HCl দ্ৰৱ এটাৰ 8 mL সম্পূৰ্ণৰূপে প্ৰশমিত কৰে । যদি আমি একেটা NaOH দ্ৰৱৰ 20 mL লওঁ তেন্তে এইখিনি প্ৰশমিত কৰিবলৈ লগা HCl দ্ৰৱৰ (আগৰ সৈতে একেটা দ্ৰৱ) পৰিমাণ হ’ব –
Answer: (a) 4 mL (b) 8 mL (c) 12 mL (d) 16 mL
Question 4: অজীৰ্ণতাৰ চিকিসাৰ বাবে তলৰ কোন ধৰণৰ ঔষধ ব্যৱহাৰ কৰা হয় ?
(a) এন্টিবায়টিক
(b) বেদনানাশক
(c) অম্লনাশক
(d) বীজাণুবাৰক
Answer: (c) অম্লনাশক
Question 5: সংঘটিত বিক্ৰিয়াৰ বাবে শব্দ সমীকৰণ আৰু সন্তুলিত সমীকৰণ লিখা যেতিয়া –
(a) লঘু ছালফিউৰিক এছিডে যিংকৰ গুড়িৰে সৈতে বিক্ৰিয়া কৰে ।
(b) লঘু হাইড্ৰ’ক্ল’ৰিক এছিডে মেগনেছিয়াম ফিটাৰে সৈতে বিক্ৰিয়া কৰে ।
(c) লঘু ছালফিউৰিক এছিডে এলুমিনিয়াম পাউদাৰৰ সৈতে বিক্ৰিয়া কৰে ।
(d) লঘু হাইড্ৰ’ক্ল’ৰিক এছিডে লোৰ গুড়িৰে সৈতে বিক্ৰিয়া কৰে ।
Answer: (a) যিংক + লঘু ছালফিউৰিক এছিড ⟶ যিংক ছালফেট + হাইড্ৰজেন
Zn + H2SO4 → ZnSO4 + H2
(b) মেগনেছিয়াম + লঘু হাইড্ৰ’ক্ল’ৰিক এছিড ⟶ মেগনেছিয়াম ক্লৰাইড + হাইড্ৰজেন
Mg + 2HCl →
MgCl2 + H2
(c) এলুমিনিয়াম + লঘু ছালফিউৰিক এছিড ⟶ এলুমিনিয়াম ছালফেট + হাইড্ৰজেন
2Al + 3H2SO4 → Al2(SO4)3
+ 3H2
(d) আইৰণ + লঘু হাইড্ৰ’ক্ল’ৰিক এছিড ⟶ ফেৰাছ ক্লৰাইড + হাইড্ৰজেন
Fe + 2HCl
→ FeCl2 + H2
Question 7: পাতিত পানীয়ে বিদ্যুৎ সৰবৰাহ নকৰে কিন্তু বৰষুণৰ পানীয়ে কৰে কিয় ?
Answer: পাতিত পানীয়ে কোনো মুক্ত আয়ন গঠন নকৰে । সেইবাবে পাতিত পানীয়ে বিদ্যুৎ সৰবৰাহ নকৰে । কিন্তু বৰষুণৰ পানীত কম-বেছি পৰিমাণে এছিড থাকে । যিহেতু এছিডৰ মাজেৰে বিদ্যুৎ প্ৰবাহিত হয় । সেয়েহে বৰষুণৰ পানীয়ে বিদ্যুৎ সৰবৰাহ কৰে ।
Question 8: পানীৰ অনুপস্থিতিত এছিডে এছিড ধৰ্ম প্ৰদৰ্শন নকৰে কিয়?
Answer: এছিডবোৰে পানীৰ লগত বিক্ৰিয়া কৰিলে হাইড্ৰজেন আয়ন উৎপন্ন কৰে। কিন্তু পানীৰ অনুপস্থিতিত এছিডে হাইড্ৰজেন আয়ন উৎপন্ন কৰিব নোৱাৰে। সেয়েহে পানীৰ অনুপস্থিতিত এছিডে এছিড ধৰ্ম প্ৰদৰ্শন নকৰে।
Question 9: পাঁচটা দ্ৰৱ A, B, C, Dআৰু E ক সাৰ্বজনীন সূচকৰে পৰীক্ষা কৰাত pHৰ মান ক্ৰমে 4,1,11,7আৰু 9 দেখুৱাইছিল। কোনটো দ্ৰৱ –
(a) প্ৰশম
(b) তীব্ৰ ক্ষাৰকীয়
(c) তীব্ৰ আম্লিক
(d) মৃদু আম্লিক
(e) মৃদু ক্ষাৰকীয়
হাইড্ৰজেন আয়নৰ গাঢ়তাৰ বৰ্ধিত ক্ৰমত pH মানবোৰ সজোৱা।
Answer: আম্লিক দ্ৰৱৰ ৰ মান 7 তকৈ কম। অন্যহাতে, ক্ষাৰকীয় দ্ৰৱৰ ৰ মান 7 তকৈ বেছি। প্ৰশম দ্ৰৱৰ ৰ মান 7 ।
(a) D প্ৰশম, কাৰণ pH =7
(b) C তীব্ৰ ক্ষাৰকীয়, কাৰণ pH =11
(c) B তীব্ৰ আম্লিক, কাৰণ pH = 1
(d) A মৃদু আম্লিক, কাৰণ pH = 4
(e) E মৃদু ক্ষাৰকীয়, কাৰণ pH = 9
হাইড্ৰজেন আয়নৰ গাঢ়তাৰ বৰ্ধিত ক্ৰমত pH মানবোৰ সজালে হ’ব –
C < E < D < A < B
Question 10: পৰীক্ষানল Aআৰু Bত সমান সমান দৈৰ্ঘ্য়ৰ দুডাল মেগনেছিয়ামৰ ফিটা লোৱা হ’ল। পৰীক্ষানল Aত হাইড্ৰক্লৰিক এছিড (HCl) আৰু পৰীক্ষানল Bত এচেটিক এছিড যোগ কৰা হ’ল। এছিড দুটাৰ গাঢ়তা একে আৰু একে পৰিমাণেই লোৱা হৈছে। কোনটো পৰীক্ষানলত বেছি বেগেৰে বুৰবুৰনি ওলাব আৰু কিয়?
Answer: Aপৰীক্ষানলত বেছি বেগেৰে বুৰবুৰণি ওলাব। কাৰণ হাইড্ৰক্লৰিক এছিড (HCl) এচেটিক এছিড তকৈ অধিক শক্তিশালী।
Question 11: কেঁচা গাখীৰৰ pH ৰ মান6 । ই দৈত পৰিণত হ’লে pH সলনি হ’বনে ? ব্য়াখ্য়া কৰা।
Answer: কেঁচা গাখীৰৰ pH ৰ মান6 হয়। ই দৈত পৰিণত হ’লে pHসলনি হ’ব। কাৰণ কেঁচা গাখীৰ দৈত পৰিণত হ’লে লেকটিক এছিড উৎপন্ন হয়। এছিডবোৰৰ pHৰ মান 6তকৈ কম হয়। সেয়ে দৈৰ pHৰ মান 6তকৈ কম হয়।
Question 12: এজন গোৱালে কেঁচা গাখীৰত সামান্য় পৰিমাণৰ বেকিং ছ’ডা যোগ কৰিলে।
(a) কিয় তেওঁ কেঁচা গাখীৰৰ pHৰ মান 6ৰ পৰা সামান্য়ভাৱে ক্ষাৰকীয় কৰি ল’লে।
(b) এই গাখীৰখিনি দৈত পৰিণত হ’বলৈ বেছি সময় লাগে কিয়?
Answer: (b) কেঁচা গাখীৰত বেকিং ছ’ডা যোগ কৰিলে ইয়াৰ ক্ষাৰকীয় গুণ কিছু পৰিমানে বাঢ়ে আৰু এছিড গুণ কমে। এছিড গুণ কম হোৱাৰ বাবে এনে গাখীৰ দৈত পৰিণত হ’বলৈ বেছি সময় লাগে।
Question 13: প্লাষ্টাৰ অব পেৰিছক জলীয় বাষ্প সোমাব নোৱাৰা পাত্ৰত থব লাগে। ব্য়াখ্য়া কৰা।
Answer: জিপছামক উষ্ণতাত উত্তপ্ত কৰিলে পানীৰ অণু হেৰুৱাই কেলছিয়াম ছালফেট হেমিহাইড্ৰেটত পৰিণত হয়। ইয়াক প্লাষ্টাৰ অব পেৰিছ বোলা হয়। ই এবিধ বগা পাউদাৰৰ দৰে। কিন্তু পানী মিহলালে ই পুনৰ জিপছামলৈ পৰিবৰ্তিত হৈ টান গোটা পদাৰ্থত পৰিণত হয়।
সেয়েহে প্লাষ্টাৰ অব পেৰিছক জলীয় বাষ্প সোমাব নোৱাৰা পাত্ৰত থব লাগে।
Question 14: প্ৰশমন বিক্ৰিয়া কি দুটা উদাহৰণ দিয়া। কাপোৰ ধোৱা ছডা আৰু বেকিং ছডাৰ দুটাকৈ গুৰুত্বপূৰ্ণ ব্য়ৱহাৰ লিখা।
Answer: এছিড আৰু ক্ষাৰকৰ মাজত বিক্ৰিয়া ঘটিলে লৱণ আৰু পানী উৎপন্ন হয়। এই বিক্ৰিয়াটোক প্ৰশমন বিক্ৰিয়া বোলা হয়। প্ৰশমন বিক্ৰিয়া এটাক তলত দিয়া ধৰণে লিখিব পাৰি –
ক্ষাৰক + এছিড → লৱণ + পানী
প্ৰশমন বিক্ৰিয়াৰ দুটা উদাহৰণ হ’ল —
(i) ছ’ডিয়াম হাইড্ৰ’অক্সাইড আৰু হাইড্ৰ’ক্লৰিক এছিডৰ মাজত বিক্ৰিয়া ঘটিলে ছ’ডিয়াম ক্লৰাইড আৰু পানী উৎপন্ন হয়। ইয়াৰ সমীকৰণটো হ’ল —
NaOH +
HCl → NaCl + H2O
(ii) পটেছিয়াম হাইড্ৰ’অক্সাইড আৰু হাইড্ৰ’ক্লৰিক এছিডৰ মাজত বিক্ৰিয়া ঘটিলে পটাছিয়াম ক্লৰাইড আৰু পানী উৎপন্ন হয়। ইয়াৰ সমীকৰণটো হ’ল –
KOH + HCl → KCl + H2O
কাপোৰ ধোৱা ছডাৰ দুটা ব্য়ৱহাৰ হ’ল —
(i) কাপোৰ ধোৱা ছডা কাঁচ, চাবোন আৰু কাগোজ উদ্য়োগত ব্য়ৱহাৰ কৰা হয়।
(ii) পানীৰ স্থায়ী কঠিনতা দূৰ কৰিবলৈ কাপোৰ ধোৱা ছডা ব্য়ৱহাৰ কৰা হয়।
বেকিং ছডাৰ দুটা ব্য়ৱহাৰ হ’ল —
(i) বেকিং পাউদাৰ প্ৰস্তুত কৰিবলৈ বেকিং ছডা ব্য়ৱহাৰ কৰা হয়।
(ii) বেকিং ছডা অগ্নি নিৰ্বাপন যন্ত্ৰত ব্য়ৱহাৰ কৰা হয়।
——————